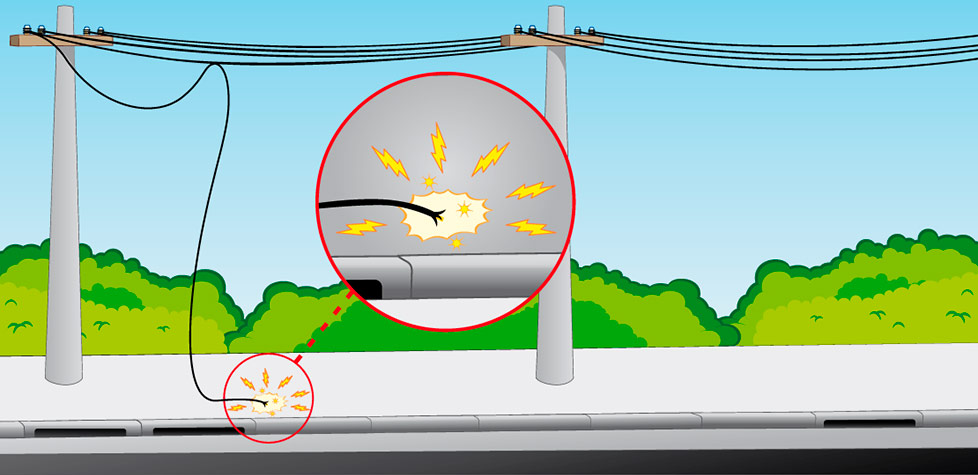
Os produtos químicos utilizados para o tratamento de água nos sistemas ou soluções alternativas coletivas de abastecimento de água para consumo humano podem introduzir à água características indesejáveis e/ou prejudiciais à saúde humana, dependendo de sua procedência ou composição. A comprovação de baixo risco à saúde (CBRS) é um documento preenchido e assinado pela empresa que está comercializando o produto químico, que comprova que determinado produto, produzido em uma unidade fabril especificada, atende aos requisitos de saúde previstos na norma e não oferece riscos à saúde, podendo ser utilizado em tratamento de água para consumo humano, quando dosado até a dosagem máxima de uso DMU ensaiada e aprovada, conforme indicada no laudo de atendimento aos requisitos de saúde (LARS) a que se refere esse documento comprobatório.
No conteúdo que deve ser apresentado no CBRS pelo uso do produto químico em tratamento de água para consumo humano, que deve ser emitido pelo fornecedor que está comercializando o produto, podem ser acrescentadas outras informações. A CBRS é específica para cada produto químico, cada concentração e cada unidade de produção discriminados no documento, e é requerido pela Portaria de Potabilidade.
Deve-se identificar a empresa que está comercializando o produto químico, no mínimo com as seguintes informações: nome e endereço; CNPJ; e inscrição estadual. Deve-se identificar o produto químico objeto da CBRS, com as seguintes informações: fabricante; identificação do produto químico; número do chemical abstracts service (CAS); unidade de produção; concentração do produto em porcentagem (%); e dosagem máxima de uso (DMU) em miligramas por litro (mg/L).
A empresa deve declarar que o produto químico que está sendo comercializado atende os requisitos estabelecidos na norma e não oferece riscos à saúde humana, quando utilizado no tratamento de água para consumo humano, desde que respeitada a DMU discriminada no documento; a CBRS do produto que está sendo comercializado está fundamentada nos resultados das análises especificadas na norma e nas suplementares definidas pelo laboratório de terceira parte responsável pela realização do relatório de estudos (RE) e pela emissão do LARS, em função das informações sobre a concentração, formulação, matérias primas e processos empregados para fabricação deste produto, que foram disponibilizadas pelo fornecedor que manipulou o produto por último, e nos demais critérios estabelecidos na norma.
Deve-se incluir, ainda, os números, as datas de emissão e de validade do RE e do LARS devem estar devidamente apresentados no conteúdo do CBRS. A CBRS deve ser datada e assinada pelo responsável técnico da empresa que está comercializando o produto, com o seu número de registro de classe. À CBRS deve ser anexada ao LARS a que se refere este documento, com o número do laudo e do estudo, bem como o nome do laboratório que o emitiu.
A NBR 15784 de 12/2023 – Produtos químicos utilizados no tratamento de água para consumo humano — Efeitos à saúde — Requisitos estabelece os requisitos para o controle de qualidade dos produtos químicos utilizados em sistemas de tratamento de água para consumo humano e os limites das impurezas nas dosagens máximas de uso indicadas pelo fornecedor do produto, de forma a não causar prejuízo à saúde humana. Esta norma se aplica aos produtos, combinações e misturas utilizadas em tratamento de água para coagulação, floculação, ajuste de pH, precipitação, controle de corrosão e incrustação, abrandamento e sequestro de íons, desinfecção e oxidação, e produtos específicos, como os utilizados para controle de algas, fluoretação, defluoretação, decloração, adsorção e remoção de cor, sabor e odor. Não se aplica aos subprodutos resultantes da reação do tratamento químico com algum constituinte da água, bem como aos materiais empregados na produção e distribuição que tenham contato com essa água.
Os produtos químicos utilizados para o tratamento de água nos sistemas ou soluções alternativas coletivas de abastecimento de água para consumo humano podem introduzir à água características indesejáveis e/ou prejudiciais à saúde humana, dependendo de sua procedência ou composição. Os requisitos de saúde para controle de qualidade dos produtos químicos utilizados em tratamento de água para consumo humano estabelecidos na norma visam o atendimento às exigências contidas na Portaria de Potabilidade vigente.
Esta norma não avalia a eficiência e o desempenho dos produtos químicos e os requisitos relativos ao odor e sabor dos produtos adicionados no tratamento de água para consumo humano. Os requisitos estabelecidos para averiguação de desempenho e eficiência dos produtos estão contidos nas respectivas normas brasileiras de especificações técnicas destes produtos.
Assim, esta norma contribui para o saneamento e a proteção da saúde pública. O fornecedor do produto deve controlar e manter registros rastreáveis no mínimo das seguintes informações: a dosagem máxima de uso (DMU) do produto; a concentração do produto; o nome comercial e número Chemical Abstracts Service (CAS) do produto; a composição da formulação (em porcentual ou partes por peso para cada componente químico da fórmula); a reação química usada para fabricar o produto, quando aplicável; as alterações na formulação; a relação das matérias primas com os respectivos fornecedores e graus de pureza de cada componente químico presente na fórmula; a fonte e o tipo de água utilizada na fabricação ou diluições posteriores do produto, bem como qualquer documentação disponível sobre o monitoramento da qualidade dessa fonte de água; as alterações de fornecedores de matéria prima; a lista de impurezas, constantes nas tabelas a norma, de acordo com o produto em análise, além daquelas passíveis de estarem presentes no produto, discriminando o percentual máximo ou partes por peso de cada uma dessas impurezas; a descrição dos processos de fabricação, manipulação e embalagem do produto; as alterações no processo produtivo; a identificação molecular (espectros ultravioletas visíveis, infravermelho, ressonância magnética e outros) para alguns produtos ou para seus principais componentes, quando requerido; e os estudos toxicológicos existentes para o produto e para as impurezas presentes no produto, publicados ou não.
Um produto químico não pode introduzir na água de consumo humano nenhuma impureza que exceda a concentração de impureza permissível por produto (CIPP), de acordo com o Anexo A, quando utilizado até a dosagem máxima de uso (DMU) recomendada. Em qualquer sistema de tratamento e distribuição de água potável, vários produtos químicos podem ser adicionados ou podem entrar em contato com a água tratada antes de sua ingestão.
A CIPP destina-se a assegurar que a contribuição total de uma única impureza de todas as fontes potenciais no sistema de tratamento e distribuição de água para consumo humano esteja dentro dos limites de concentração aceitáveis, conforme o Anexo A. Na ausência de informações específicas quanto ao número de fontes potenciais de impurezas, deve ser adotado um fator de segurança (FS) igual a dez, admitindo-se um limite de 10% do valor máximo permitido (VMP) como contribuição de uma determinada impureza contida em cada produto.
O fator de segurança utilizado nesta norma está de acordo com o critério do US National Research Councile. A concentração de impurezas para cada produto químico individual (CIPA) não pode ser superior aos limites estabelecidos no Anexo A (CIPP). Para mistura de produtos químicos, cujos componentes tenham atendido aos requisitos estabelecidos na norma como produtos individuais, a concentração de impurezas provenientes de cada componente da mistura não pode ser superior aos limites estabelecidos no Anexo A.
Para mistura de produtos químicos, cujos componentes não tenham atendido aos requisitos estabelecidos na norma, a concentração das impurezas da mistura não pode exceder os limites estabelecidos no Anexo A. Para a mistura, deve-se considerar a possibilidade de a concentração das impurezas nos produtos individuais vir a ser alterada pelo seu uso em mistura.
Para mistura de produtos químicos, o método de preparação da amostra deve ser selecionado de acordo com os métodos de cada produto da mistura. Por exemplo, uma mistura de ácido fosfórico e outra espécie diferente de fosfato é preparada utilizando o método D para análise das impurezas do ácido fosfórico, enquanto que o método B é usado para a análise das impurezas contidas na espécie de fosfato. Alíquotas separadas são usadas para a análise de cada componente da mistura.
Para produtos químicos gerados no local de aplicação, a exemplo do dióxido de cloro e das cloraminas, a concentração de impurezas provenientes de cada componente dos produtos químicos utilizados para a sua geração não pode ser superior aos limites estabelecidos no Anexo A. Para o processo de avaliação do produto químico, o patrocinador, dentro de um acordo de confidencialidade e por unidade de produção, deve apresentar ao laboratório de terceira parte que realiza o estudo, as informações contidas na norma para o produto químico em estudo.
O patrocinador deve informar a concentração do produto químico, objeto do estudo ao laboratório de terceira parte, por unidade de produção, conforme a norma. Para produto químico que possuir norma brasileira de especificação técnica para uso em tratamento de água para consumo humano, onde são definidas faixas de concentração, o estudo deve ser realizado para qualquer valor ou faixa declarado pelo fornecedor, e deve ser aceito desde que esteja contido nessa faixa de especificação.
Para produto químico que possuir norma brasileira de especificação técnica para uso em tratamento de água para consumo humano, onde são definidos apenas valores mínimos de concentração, o estudo deve ser realizado e aceito para valor igual ou superior ao especificado, conforme declarado pelo fornecedor. Para produto químico que possuir norma brasileira de especificação técnica para uso em tratamento de água para consumo humano, cujo valor de concentração declarado pelo fornecedor não esteja previsto nesta norma, esse valor deve ser informado no estudo a ser realizado e deve ser aceito.
Para produto químico comercializado que não possuir norma brasileira de especificação técnica para uso em tratamento de água para consumo humano, a concentração declarada pelo fornecedor deve ser informada no estudo. O patrocinador deve informar a DMU do produto químico, por unidade de produção, que deve ser considerada no estudo a ser realizado pelo laboratório de terceira parte.
O laboratório de terceira parte deve realizar a coleta da amostra conforme definido na norma. O laboratório de terceira parte deve elaborar um plano de estudos em boas práticas de laboratório (BPL), para cada produto, por unidade de produção, considerando todas as informações prestadas pelo patrocinador conforme a norma, contendo todos os analitos específicos relacionados nas tabelas da norma, adicionando outros ensaios necessários, em função da formulação, das matérias-primas empregadas e do processo de fabricação do produto químico em análise. O plano de estudos deve ser elaborado conforme legislação vigente.
O laboratório de terceira parte deve verificar a compatibilidade do método de preparação da amostra com o método de análise do analito desejado. Após a realização do estudo em BPL e a elaboração do relatório de estudos (RE), o laboratório de terceira parte deve emitir o laudo de atendimento aos requisitos de saúde (LARS) conforme requerido pela Portaria de Potabilidade vigente, contendo as informações discriminadas no Anexo B.
O fornecedor que está comercializando o produto químico deve preencher e disponibilizar a comprovação de baixo risco à saúde (CBRS) pelo uso do produto químico em tratamento de água para consumo humano, específico para cada produto e para cada unidade de produção, conforme requerido pela Portaria de Potabilidade vigente, contendo as informações discriminadas no Anexo C. O LARS e o CBRS devem ser emitidos respectivamente pelo laboratório de terceira parte e pelo fornecedor que está comercializando, por produto, na concentração declarada, conforme unidade de produção e dosagem máxima de uso (DMU) informada pelo patrocinador.
O RE e o LARS possuem validade máxima de dois anos, sendo obrigatória a repetição do estudo após este período. Caso haja alteração na matéria-prima, na formulação ou no processo produtivo, que alterem a composição final do produto, o patrocinador deve providenciar um novo RE para emissão de um novo LARS, ainda que o prazo máximo de dois anos não esteja excedido.
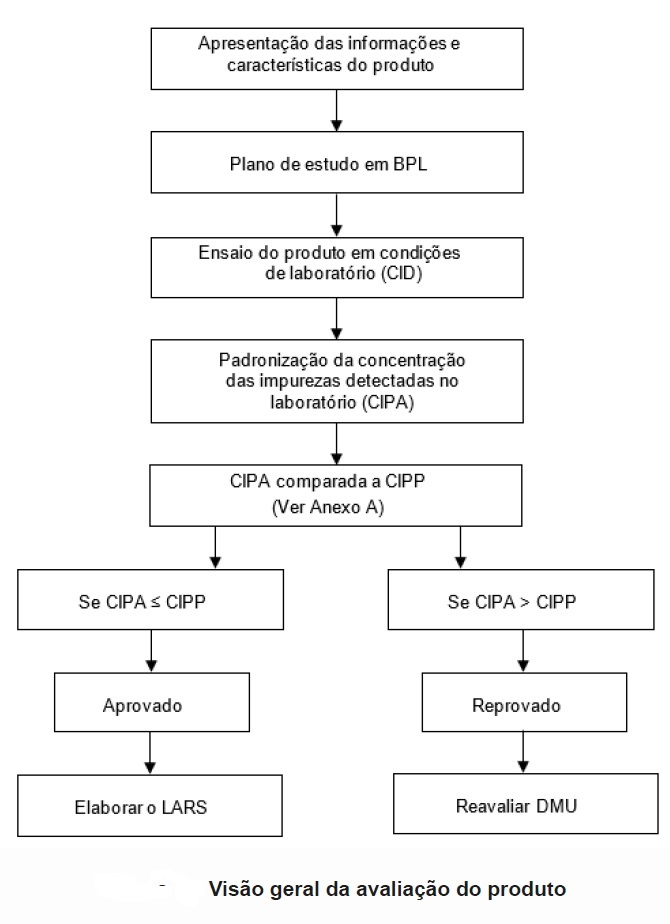
A figura abaixo apresenta uma visão geral do processo de avaliação de um determinado produto químico. Em função dos resultados obtidos na avaliação, o produto pode ou não ser aprovado para aquela dosagem máxima sugerida pelo patrocinador, para uma determinada unidade de produção. Para isso, a CIPA de cada impureza não pode ser superior aos limites da concentração de impureza permissível por produto (CIPP), conforme o Anexo A.
Um produto químico específico aprovado para uma determinada DMU, conforme o que estabelece esta norma, também deve ser considerado aprovado para valor de DMU inferior, quando o produto for de mesma especificação, produzido na mesma unidade e possuir a mesma concentração do produto que foi ensaiado e aprovado pelo laboratório de terceira parte no RE e declarado no LARS. Os produtos químicos não contemplados nesta norma e na NSF/ANSI/CAN 60 devem ser avaliados de acordo com as informações apresentadas pelo patrocinador e nos critérios de avaliação de risco adotados na NSF/ANSI/CAN 600 ou em outros documentos reconhecidos para aprovação do seu uso.
Quanto à amostragem, a amostra deve ser coletada em ponto antes do embarque e deve ser representativa do produto comercializado. Nenhuma amostra pode ser coletada de contentores danificados ou com vazamentos. A amostragem deve ser realizada pelo laboratório responsável pelo estudo em BPL ou pelo fornecedor com acompanhamento de técnico deste laboratório.
A amostragem deve ser representativa e realizada no último ponto de manipulação do produto, e o procedimento deve ser documentado com as observações e registros fotográficos, de filmagem e outros registros pertinentes que evidenciem o momento da coleta. A amostra deve ser lacrada e codificada numericamente com o dispositivo fornecido pelo laboratório e identificada para assegurar a rastreabilidade do processo.
O laboratório responsável pelo estudo em BPL deve dispor de procedimento com a descrição dos requisitos para acompanhamento da amostragem, com os fatores a serem controlados para assegurar a validade da amostragem e resultados subsequentes. O acompanhamento da amostragem pode ser feito de forma presencial ou remota.
A decisão sobre o modo de acompanhamento e a justificativa para a adoção de um formato ou outro devem ser documentadas pelo laboratório nos registros da amostragem. Caso o acompanhamento da amostragem seja conduzido de forma remota, deve ser feito por meio de plataformas adequadas e desenvolvido de forma síncrona (em tempo real) durante o momento da amostragem, e assíncrona para avaliação de registros e documentos envolvidos no processo de amostragem.
As evidências da amostragem devem ser registradas por meio de documentos, fotos e vídeos e arquivadas pelo laboratório. O acompanhamento remoto da amostragem deve ser online e pode ser realizado em formato de reuniões na web, teleconferências, serviços de vídeo com áudio on-line ou técnicas digitais similares mais inovadoras.
O fornecedor deve referenciar ao laboratório o profissional responsável por facilitar o processo de acompanhamento remoto da amostragem. Todas as considerações logísticas e técnicas necessárias para assegurar que os envolvidos e os recursos adequados estejam disponíveis nos horários solicitados pelo laboratório devem ser observadas e providenciadas por este profissional.
Para produtos a granel, devem ser coletadas cinco amostras individuais com aproximadamente 100 mL cada uma, de várias profundidades e seções do recipiente de armazenagem. As amostras individuais devem ser compostas e homogeneizadas para formar uma única amostra com cerca de 500 mL.
Para produtos embalados, deve ser coletada uma amostra composta dos lotes, por meio da seleção aleatória de amostras individuais de aproximadamente 5% dos recipientes do lote com no mínimo, cinco e no máximo 15 recipientes amostrados. Se houver menos de cinco recipientes, os procedimentos de amostragem devem ser idênticos àqueles usados para recipientes a granel. As amostras individuais devem ser compostas e homogeneizadas para formar uma única amostra de cerca de 500 mL.
Filed under: amostragem, atendimento ao cliente, Atendimento ao consumidor, avaliação de conformidade, Defesa do consumidor, direito do cidadão, gestão da qualidade, gestão em saúde, normalização | Leave a comment »