Um cell-based health care products (CBHP) ou os produtos para saúde baseados em células são aqueles que contêm ou consistem em células pró ou eucarióticas ou entidades biológicas derivadas de células como um ingrediente essencial. Um processo de determinação de risco do material de início baseado em células deve ser definido e implementado.
Para determinação de risco de materiais viáveis de origem humana, a ISO 13022 deve ser aplicada. Para determinação de risco de materiais de origem animal, a ISO 22442 (todas as partes) deve ser aplicada. Para materiais de origem vegetal, agentes infecciosos (por exemplo, micoplasma, bactérias, fungos, leveduras, protozoários e vírus) devem ser considerados conforme os requisitos regulatórios locais.
Reconhece-se que pode existir contaminação biológica intrínseca nos materiais de partida. Os critérios de aceitação associados a tal contaminação nos materiais de partida devem ser estabelecidos e confirmados na determinação de risco, documentados na especificação do material de partida e tratados na validação do processo e nos critérios de liberação.
Durante o projeto e desenvolvimento de um processo de CBHP, a determinação de risco deve ser usada para identificar e quantificar os perigos de contaminação biológica para cada etapa do processo, a fim de evitar contaminação cruzada. Isso inclui a entrada de contaminação biológica extrínseca e disseminação de contaminação biológica intrínseca.
Os procedimentos de atenuação devem ser implementados quando identificados como necessários. Tanto a quantificação do risco de contaminação quanto a verificação da eficácia dos procedimentos de atenuação devem ser determinadas e controladas.
Estes procedimentos devem incluir o controle de contaminação biológica intrínseca do produto, incluindo microrganismos especificados, a contaminação biológica extrínseca do produto ou ambiente de fabricação, e o monitoramento de particulado do ambiente (viável e não viável), dependendo do nível de limpeza. A determinação de risco deve ser usada para projetar a simulação do processo para produtos processados assepticamente, como nas NBR ISO 13408 1 e ISO 13408 7.
A simulação do processo é empregada para verificar se o risco residual geral de contaminação microbiana extrínseca de todo o processo é aceitável. O processo do CBHP pode ser simulado em um processo contínuo ou pode ser dividido em duas ou mais etapas para efeitos de simulação de processo, por exemplo, empregando duas ou mais abordagens diferentes para simulação de processo com base nas etapas do processo, desde que todo o processo seja simulado.
Para produtos não estéreis ou produtos em que as etapas de controle de contaminação biológica são necessárias, a determinação de risco do material de partida deve ser usada para projetar estudos de simulação e/ou confirmação de processo. Os resultados da determinação de risco podem ser usados no projeto de simulação de processo e/ou estudos de confirmação de processo (quando aplicável) para demonstrar que o processo evita a contaminação extrínseca e que a contaminação intrínseca está controlada.
A aplicação da determinação de risco e do ensaio biológico é, geralmente, um processo iterativo. À medida que o processo se desenvolve e se aprimora ainda mais, a simulação do processo do CBHP deve ser modificada, quando necessário, para assegurar que reflita todo o processo.
A determinação de risco original deve ser revisada e, quando necessário, modificada, para assegurar que todos os riscos associados ao processo sejam identificados, avaliados e controlados. A integridade do fechamento do recipiente da embalagem primária deve ser avaliada.
O desenvolvimento e a qualificação do processo de produção dos CBHP para ensaios clínicos devem seguir os requisitos regulatórios nacionais ou regionais. Quando considerado necessário, e com base na definição do processo e na avaliação de risco, serão estabelecidos os requisitos especiais de contenção para material de partida não estéril adquirido.
Uma sala de aquisição deve ser instalada para material de partida não estéril que seja processado por subcontratados. A qualificação, requalificação e manutenção do nível de contenção e das instalações de contenção estabelecidas na sala de aquisição serão especificadas nos procedimentos. Os requisitos devem seguir os requisitos de boas práticas aplicáveis (por exemplo, boas práticas de fabricação, boas práticas de tecido).
O estado de descontaminação e o estado de quarentena devem ser verificados antes da transferência do material de partida para a área de fabricação. Os resultados dos testes para a contaminação biológica intrínseca devem estar em conformidade com os requisitos de especificação do material de partida. O transporte de material de partida não estéril para as áreas de processamento de célula (APC) ou áreas de processamento asséptico (APA) deve ser realizado de acordo com os requisitos de contenção controlada.
A NBR ISO 18362 de 08/2023 – Fabricação de produtos para saúde baseados em células — Controle de riscos microbianos durante o processamento especifica os requisitos mínimos e fornece orientação sobre uma abordagem baseada em risco para o processamento de produtos para saúde baseados em células (cell-based health care products – CBHP) que requerem controle de contaminação microbiana viável e não viável. É aplicável tanto aos CBHP rotulados como estéreis quanto aos CBHP não rotulados como estéreis.
Esta norma não é aplicável a: aquisição e transporte de material de início baseado em células usado no processamento de um CBHP, banco de células, controle de material genético, controle de contaminação de produto não microbiano, diagnósticos in vitro (IVD) ou — medicamentos naturais. Exemplos: vitaminas e minerais, remédios de ervas, remédios homeopáticos, remédios tradicionais, como remédios tradicionais chineses, probióticos, outros produtos como aminoácidos e ácidos graxos essenciais. Esta Norma não define os requisitos de contenção de biossegurança e não substitui os regulamentos nacionais ou regionais que se aplicam à fabricação e controle de qualidade de um CBHP.
Um produto para saúde baseado em células (CBHP) compreende células procarióticas ou eucarióticas, ou entidades biológicas derivadas de células como um ingrediente essencial. O material de início baseado em células ou derivado de células usado na fabricação de um CBHP pode ser viável ou não viável e de origem humana, animal, microbiana ou vegetal.
Uma característica comum dos CBHP é que sua eficácia é baseada em suas propriedades biológicas. Eles são classificados como medicamentos, produtos para saúde, biológicos ou produtos combinados, dependendo das regulamentações internacionais, nacionais e/ou regionais que regem o fornecimento desses produtos.
Os CBHP podem ser limitados em sua capacidade de resistir aos métodos de esterilização e purificação. Esta norma internacional foca no processo em vez de no produto. Descreve os elementos mínimos necessários para uma abordagem baseada no risco para o processamento de um CBHP, a fim de reduzir o potencial de aumento da contaminação intrínseca do produto e evitar a contaminação extrínseca do produto.
O projeto dos processos, equipamentos, instalações, utilidades, as condições de preparação e adição de tampões e reagentes e o treinamento dos operadores são considerações fundamentais para minimizar a contaminação. Um CBHP que é rotulado como estéril é esterilizado por um processo de esterilização terminal ou é processado assepticamente. Exemplos de CBHP que são esterilizados terminalmente incluem, mas não se limitam a, osso esponjoso, matriz óssea desmineralizada, suturas de categute, válvulas cardíacas biológicas e remendos de tecido.
A garantia de esterilidade para esses CBHP é obtida por meio de um projeto adequado e do controle do ambiente, dos controles sobre materiais de início e de embalagem, de um projeto adequado e de qualificação de processos de fabricação, incluindo o processo de esterilização terminal e a aplicação de controles e ensaios apropriados durante o processo. Requisitos e orientações para esterilização terminal de CBHP estão contidos nas NBR ISO 17665 1, ABNT ISO/TS 17665-2, ISO 11137 1, NBR ISO 11137 2, ISO 11137 3, NBR ISO 11135, ISO 14160, NBR ISO 20857, NBR ISO 14937 e NBR ISO 25424, conforme aplicável.
Os controles de alguns agentes infecciosos (por exemplo, vírus e protozoários) podem requerer uma abordagem multifacetada para garantir a qualidade e segurança do produto. Esses agentes não são considerados especificamente nas normas existentes para esterilização finalizada ou processamento asséptico. Um CBHP que é rotulado como estéril e que não pode ser esterilizado terminalmente é processado assepticamente.
A garantia de esterilidade para esses CBHP é obtida por meio de um projeto adequado e controle do ambiente, controles sobre materiais de início e embalagens, projeto adequado e qualificação de processos de fabricação, simulação de processo (conforme os requisitos da série ISO 13408), da aplicação de controles apropriados durante o processo de fabricação e ensaios para demonstrar a obtenção das condições de processamento asséptico. Como pré-requisito, os materiais de início e os materiais de embalagem são esterilizados por processos validados.
Nesse sentido, esta norma não reitera requisitos para processos específicos que são usados durante o processamento de um CBHP que é rotulado como estéril. Para um CBHP que é fornecido sem uma declaração de esterilidade no rótulo, por exemplo, tecido da córnea ou enxertos de pele viáveis, o processamento envolve o uso de técnicas assépticas adequadas em todas as fases durante o processo.
Os componentes podem estar sujeitos à redução da bioburden (carga microbiana) durante a preparação anterior à sua montagem ou combinação para formar o produto acabado. Isso é necessário para minimizar o potencial de aumento da contaminação intrínseca do produto durante o processamento e para evitar a contaminação extrínseca do produto.
Os controles e técnicas para manter a qualidade do produto durante o processamento desses CBHP podem ser diferentes daqueles usados para o processamento de um CBHP rotulado como estéril. Os controles de alguns agentes infecciosos, por exemplo, vírus e protozoários, podem exigir uma abordagem multifacetada para garantir a qualidade e segurança do produto.
A garantia de qualidade microbiológica para um CBHP que é fornecido sem uma declaração de esterilidade no rótulo é obtida mediante o controle do meio ambiente, controles sobre os materiais de início e embalagem, projeto adequado e qualificação de processos de fabricação, confirmação de processo e estudos de simulação de processo e aplicação de controles e ensaios em processo. A determinação de risco fundamenta a seleção de critérios de qualidade microbiológica adequados para um CBHP que é fornecido sem uma declaração de esterilidade no rótulo.
Esses critérios definem a aceitabilidade do produto com base na ausência ou presença, ou número de microrganismos, por quantidade definida de produto, para garantir que o produto acabado não represente risco microbiológico para o paciente. Dependendo das especificações do produto final, o processamento dos CBHP pode envolver muitas operações individuais que precisam ser efetivamente combinadas e controladas para: minimizar o potencial de contaminação biológica intrínseca no material de partida, limitar a proliferação de contaminação biológica intrínseca no processo, evitar contaminação biológica extrínseca do produto, e assegurar um produto acabado com características biológicas definidas.
O objetivo da escolha do processo é obter uma compreensão abrangente da integração de todos os elementos diferentes necessários para a fabricação do CBHP com sucesso e segurança. Os elementos típicos são apresentados no Anexo F. A escolha do processo para um CBHP deve ser conduzida após a especificação do material de partida e a especificação do produto terminado do CBHP terem sido estabelecidas.
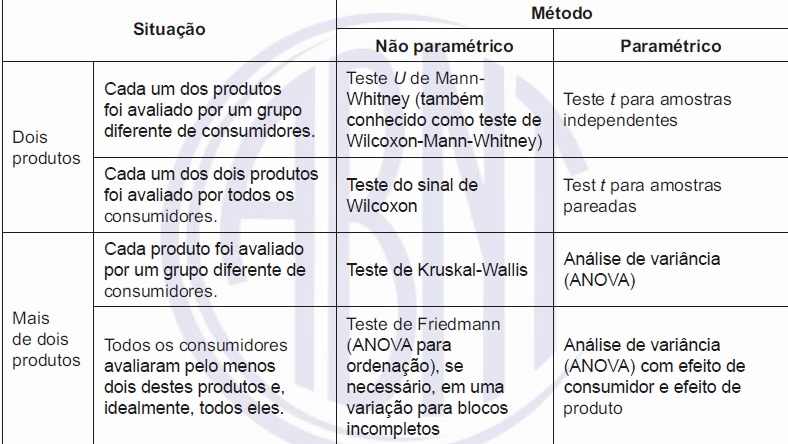
Os critérios de aceitação estabelecidos nestes documentos devem ser usados como requisitos de entrada. Quando um CBHP é esterilizado por um processo de esterilização terminal, a NBR ISO 14937, a série ISO 11137, a NBR ISO 17665 1, a NBR ISO 20857, a ISO 14160, a NBR ISO 11135 e a NBR ISO 25424 (conforme aplicável), devem ser seguidas. Consideração específica deve ser dada à análise sistemática de materiais de partida baseados em células para identificar o risco de contaminação microbiana no curso do processamento (ver tabela abaixo), análise sistemática do potencial de introdução de contaminação microbiana extrínseca ao processo, e o desenvolvimento de estudos de confirmação de processo (por exemplo, tratamento de pré-esterilização de bioburden).

Quando um CBHP é destinado a ser estéril e não pode ser esterilizado terminalmente, este CBHP deve ser processado assepticamente. As NBR ISO 13408-1 e ISO 13408-7 (conforme aplicável) devem ser seguidas. Uma consideração específica deve ser dada à análise sistemática de materiais iniciais baseados em células para identificar o risco de contaminação microbiana no curso do processamento (ver tabela acima).
Quando um CBHP não puder ser esterilizado terminalmente ou processado assepticamente, os critérios a seguir devem ser aplicados: análise sistemática de materiais de partida baseados em células para identificar o risco de contaminação microbiana intrínseca no curso do processamento; análise sistemática do potencial de introdução de contaminação microbiana extrínseca no processo; e o desenvolvimento de estudos de confirmação de processo.
Com base na definição do processo CBHP, será realizada uma avaliação dos riscos de processamento. Métodos e/ou procedimentos para minimizar e controlar esses riscos devem ser descritos e implementados. Riscos residuais devem ser justificados. Exemplos de riscos específicos de processo associados ao CBHP incluem: uso de material de partida com contaminação biológica intrínseca, inativação insuficiente (ou aumento seletivo) de contaminação biológica intrínseca, ingresso de contaminação extrínseca, inativação de atividade biológica e liberação acidental de material perigoso de uma instalação de contenção.
A definição do processo deve considerar o processo completo e fornecer uma justificativa descrevendo como cada elemento envolvido no processamento contribui para a obtenção da especificação do produto. A definição do processo deve ser documentada e aprovada pelo pessoal designado. A definição do processo deve ser revista sempre que ocorrer uma mudança.
Uma orientação sobre a identificação de atributos críticos de qualidade, parâmetros de processo e atributos de material, que são necessários no desenvolvimento de uma definição de processo, é fornecida no ICH Q8. Para materiais usados durante o processamento de CBHP, deve-se considerar a prevenção, remoção ou inativação de contaminantes durante o processo de determinação de risco.
Um processo de gerenciamento de risco deve ser definido e implementado conforme as NBR ISO 14971 e ICH Q9. A determinação de risco deve ser conduzida para identificar e avaliar os riscos associados ao processamento e os riscos associados ao CBHP específico, e para entender a interação desses riscos.
Os resultados da determinação de risco devem ser usados como dados de entrada para medidas de atenuação de risco e para projetar simulação de processo e estudos de confirmação de processo. Os riscos de contaminação biológica intrínseca causados por materiais de partida baseados em células e sua contribuição para os riscos de contaminação cruzada entre lotes são de grande importância no processamento de CBHP.
Filed under: avaliação de conformidade, Defesa do consumidor, direito do cidadão, estratégia, gestão de fornecedores, gestão em saúde, Indicadores de desempenho, infecção hospitalar, Informação científica, normalização | Leave a comment »